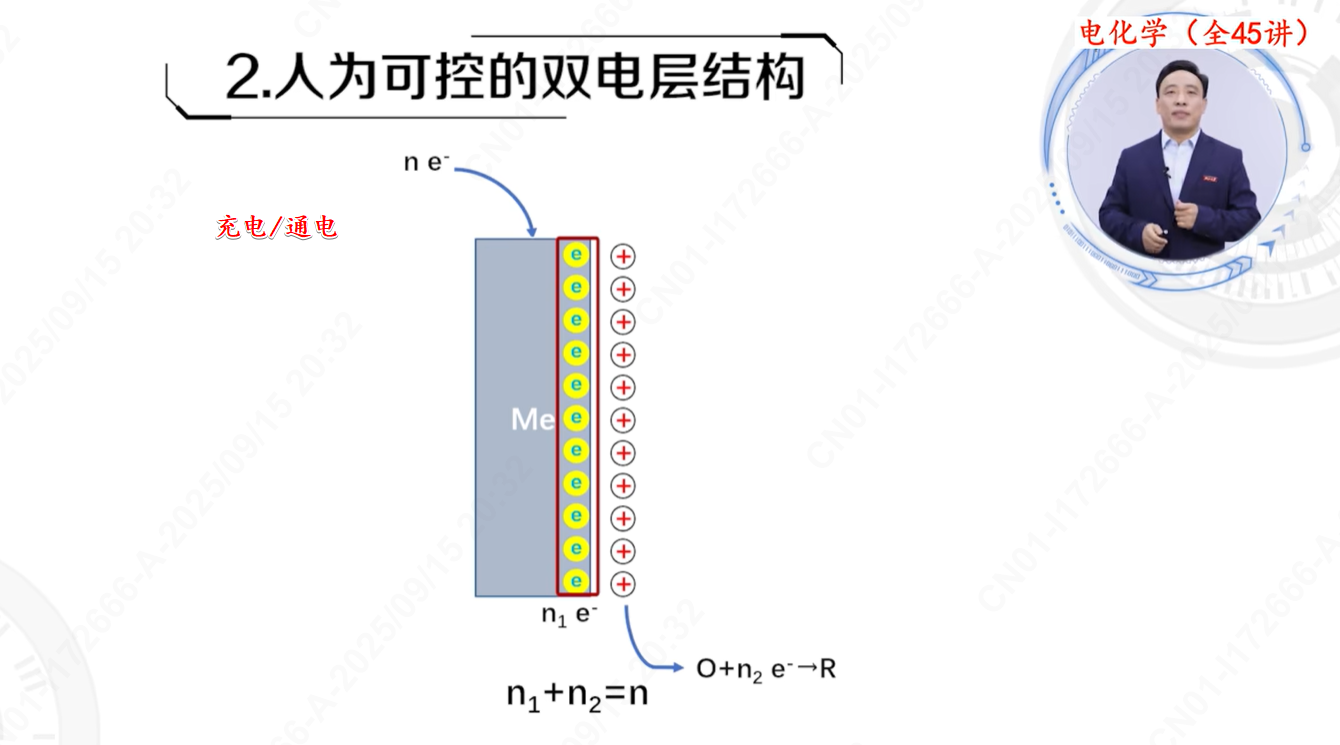
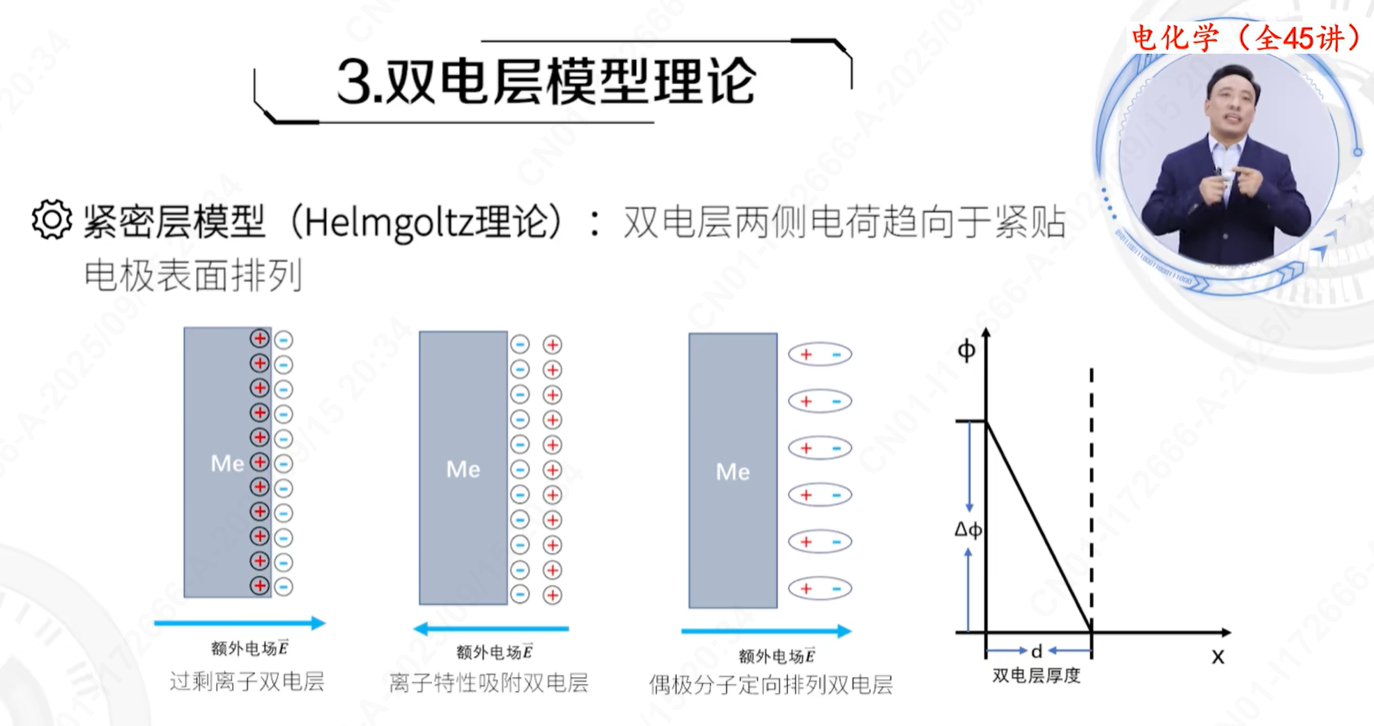
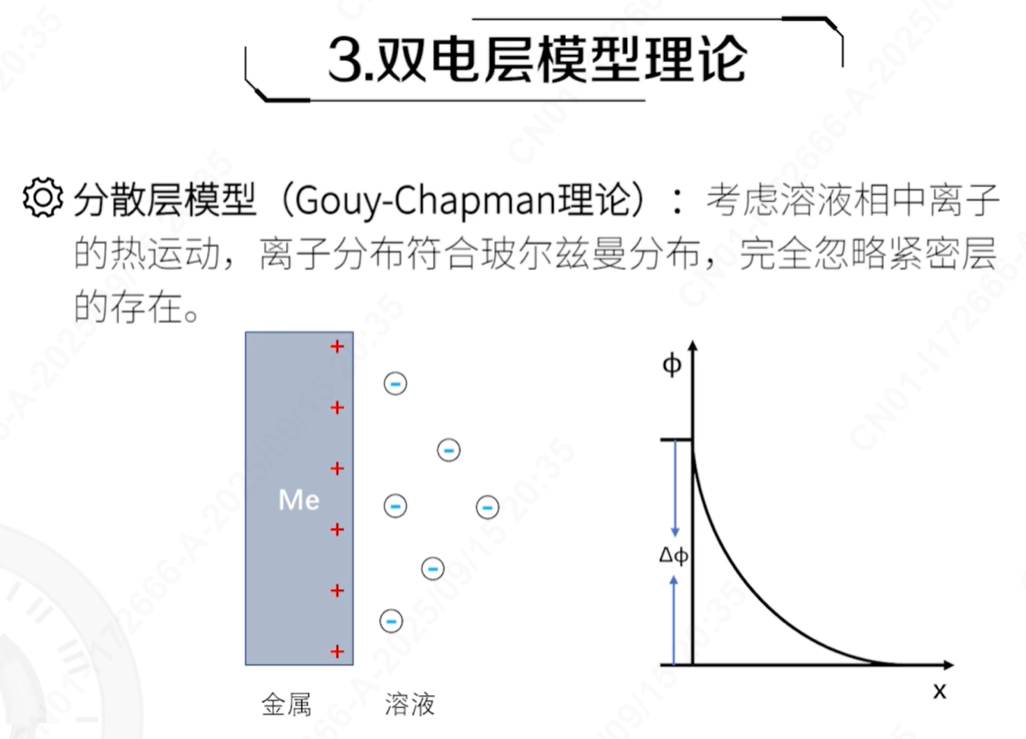
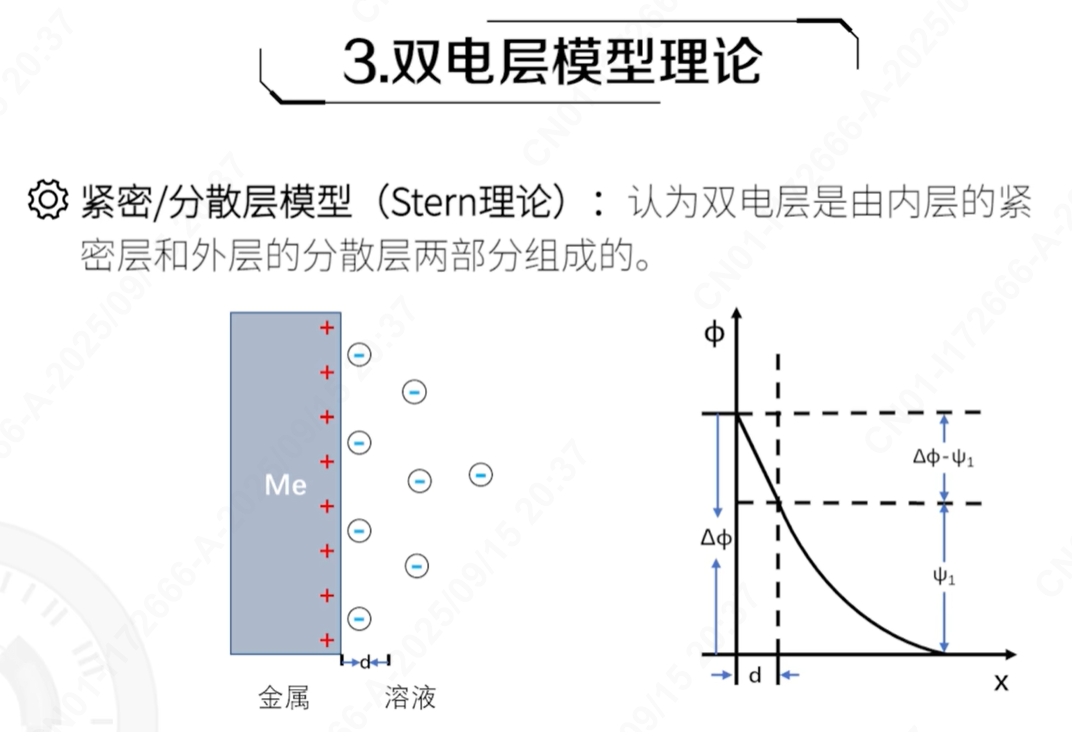
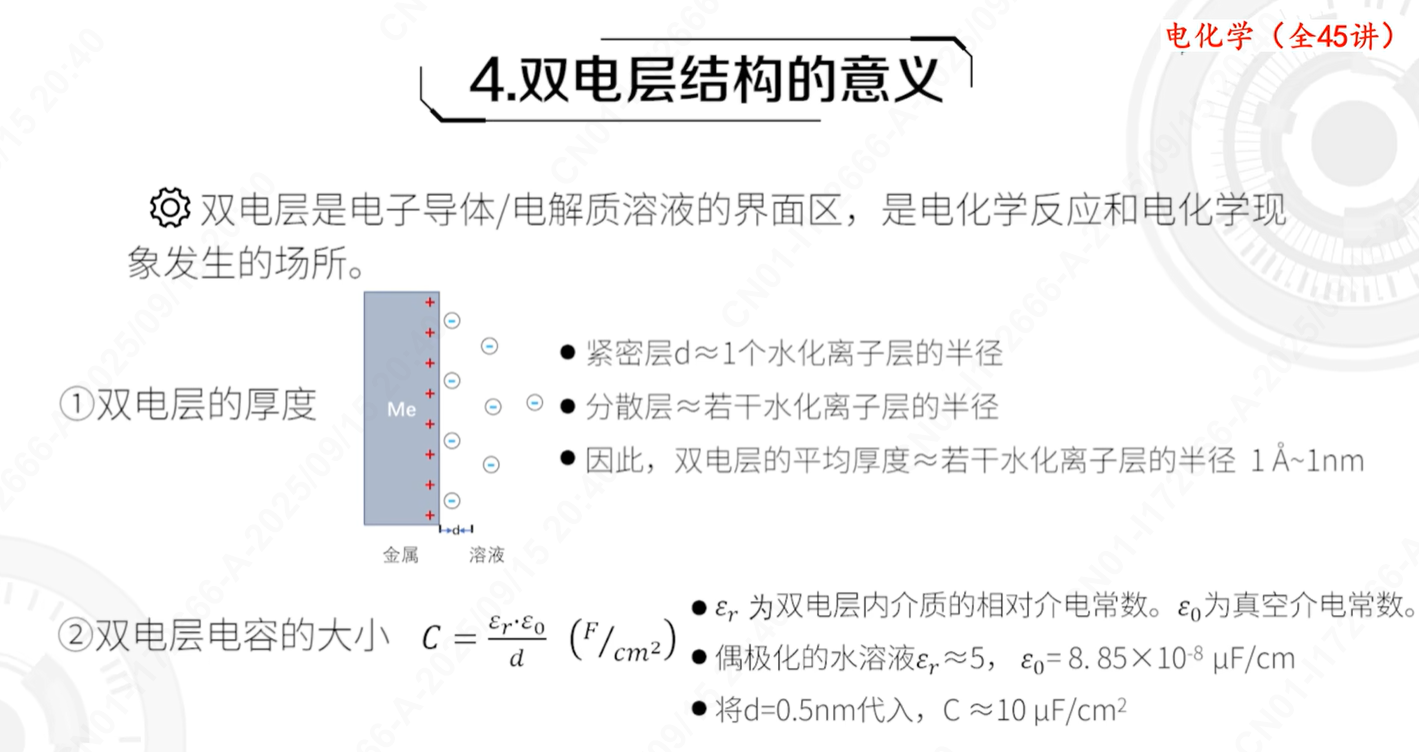
理论
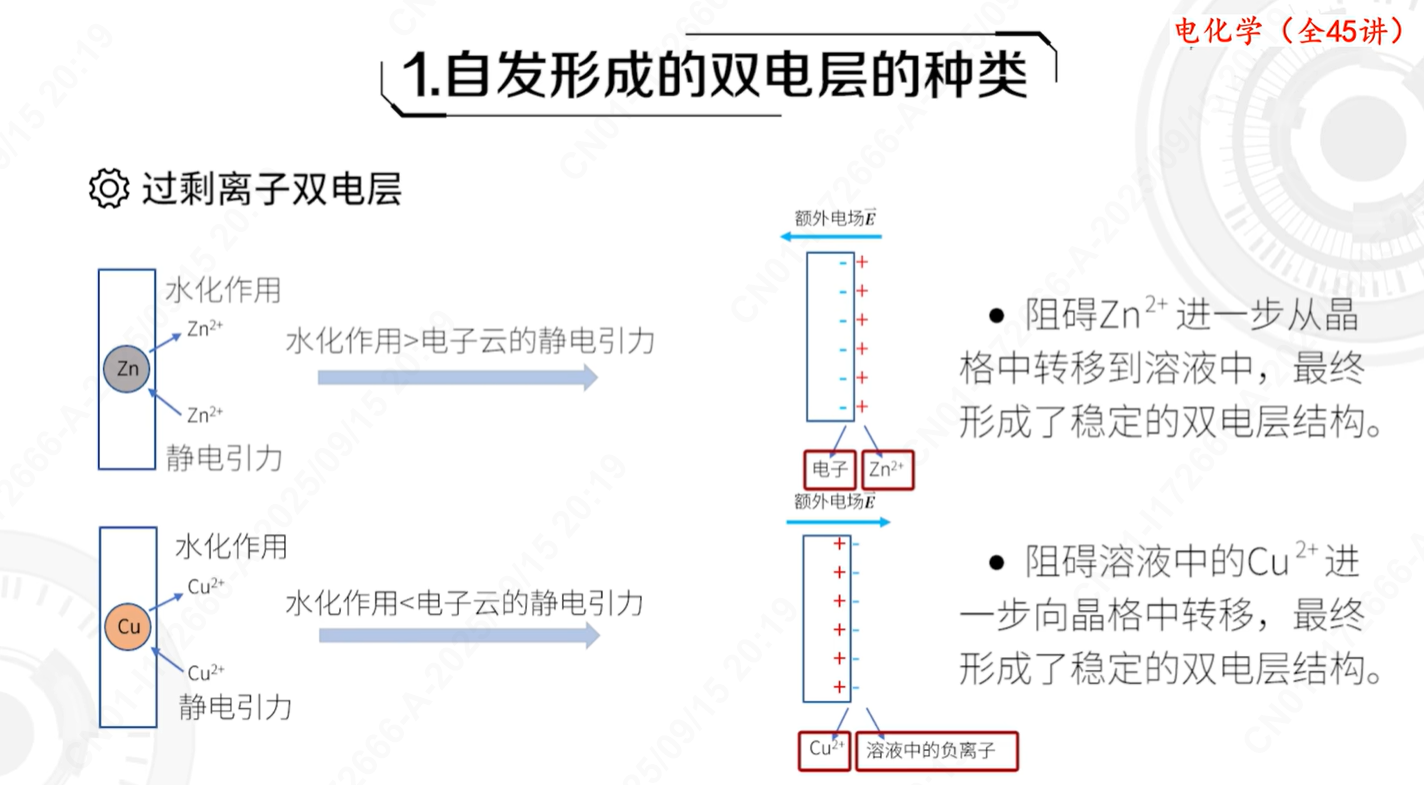
水化作用的本质是水分子通过氢键、静电力或配位键等作用力与物质结合。当离子或分子溶于水时,会破坏水原有的四面体氢键结构,并在其周围形成定向排列的水分子层,称为水化膜。这个过程属于“溶剂化”的一种(以水为溶剂时特称为水化),它促进了物质的溶解或离解。
在电解质溶液中,离子通常以水化离子的形式存在,例如 Cu²⁺ 会形成 [Cu(H₂O)₄]²⁺ 这样的配位离子。
电子云与静电引力的基本概念
要理解"电子云的静电引力",首先需要知道"电子云"和"静电引力"分别是什么:
电子云:在原子中,电子并非像行星绕太阳那样有固定的轨道,而是以“概率云”的形式分布在原子核周围。你可以把它想象成一层带负电的、不断运动的“云雾”,笼罩在带正电的原子核周围。这层“云雾”的密度分布代表了电子在某个区域出现的概率。
静电引力:指的是带有相反电性的电荷之间会产生相互吸引的力。它的规律是:引力的大小与两个电荷量的乘积成正比,与它们之间距离的平方成反比(即著名的库仑定律)。
“电子云的静电引力” 描述的就是一个原子的电子云(整体呈负电性)与另一个带正电的物体(或物体带正电的部分)之间的这种相互吸引的力。


极性分子的含义:当一个分子内部正电荷中心与负电荷中心不重合时,就形成了所谓的偶极矩(可以理解为分子极性的强弱),这样的分子就是极性分子。
一个水分子(H₂O)由一个氧原子和两个氢原子通过共价键结合而成。这三个原子的排列并非直线,而是呈现一个V形或者说是角形结构,两个O-H键之间的夹角约为104.5度。
氧原子的电负性(吸引电子的能力)比氢原子强得多。这意味着在形成共价键时,共享的电子对会更偏向氧原子一方。结果就是:
-
氧原子一端:由于电子云密度较高,因而带有部分负电荷(用δ-表示)。
-
氢原子一端:相对失去电子,因而带有部分正电荷(用δ+表示)。